Asam dan Basa
Asam berasal dari bahasa latin, yaitu "denfan ktaacidus" yang artinya masam. Asam adalah senyawa yang sering terkandung pada buah-buahan seperti jeruk dan mangga. Rasa asam sebenarnya adalah senyawa kimia yang dapat larut di dalam air. Senyawa asam membuat pH air menjadi lebih kecil dari 7.
⇢ Sifat:




⇢ Sifat:
- Rasa: Masam atau kecut dalam Bahasa Jawa jika dilarutkan dalam air.
- Sentuhan: Asam yang sangat pekat akan terasa menyengat jika terkena kulit, bahkan dapat merusak sel kulit.
- Kereaktifan: Asam dapat bereaksi dengan baik jika bertemu dengan logam. Bahkan dapat membuat logam lama-lama mengalami korosi.
- Hantaran listrik: Larutan asam adalah larutan elektrolit yang sangat baik dalam fungsinya sebagai konduktor elektrik.
⇢ Pengelompokan:
- Asam kuat, yaitu asam yang banyak menghasilkan ion yang ada dalam larutannya (asam yang terionisasi sempurna dalam larutannya).
- Asam lemah, adalah asam yang sedikit menghasilkan ion yang ada dalam larutannya (hanya terionisasi sebagian).
⇢ Contoh:
- Asam Kuat :
- Asam klorida (HCl)
- Asam nitrat (HNO3)
- Asam sulfat (H2SO4)
- Asam bromida (HBr)
- Asam iodida (HI)
- Asam lemah :
- Asam format (HCOOH)
- Asam asetat (Asam cuka) (CH3COOH)
- Asam fluorida (HF)
- Asam karbonat (H2CO3)
- Asam sitrat (C6H8O7)
Basa adalah senyawa yang banyak digunakan dalam campuran sabun mandi atau sabun cuci. Secara kimia, basa adalah senyawa yang menyerap iom hidronium ketika dilarutkan ke dalam air. Basa adalah lawan dari asam. Jika kedua larutan asam dan basa disatukan akan saling menetralkan. Jika larut dalam air maka pH larutan akan menjadi lebih dari 7.
⇢ Sifat:
- Rasa: Cenderung pahit jika dirasakan dengan lidah.
- Sentuhan: Basa akan terasa licin jika disentuh dan bercampur dengan air. Seperti sabun yang sering kita gunakan.
- Kereaktifan: Basa juga dapat menyebabkan pelapukan pada logam seperti layaknya asam.
- Hantaran listrik: Larutan basa adalah larutan elektrolit yang berfungsi sebagai konduktor elektrik.
⇢ Pengelompokan:
Dari kuat atau tidaknya maka basa dibagi menjadi dua jenis yaitu basa kuat yang sering disebut kostik dan basa lemah. Kemampuan ini didasarkan pada kemampuan melepaskan ion OH– dalam larutan dan juga konsentrasi larutan yang dihasilkan.
- Basa kuat, yaitu basa yang bisa menghasilkan ion OH dalam jumlah yang besar. Basa kuat biasanya disebut dengan istilah kausatik.
- Basa lemah, yaitu basa yang bisa menghasilkan ion OH dalam jumlah kecil.
⇢ Contoh:
- Basa kuat :
- Litium hidroksida (LiOH)
- Natrium hidroksida (NaOH)
- Kalium hidroksida (KOH)
- Kalsium hidroksida (Ca(OH)2)
- Rubidium hidroksida (RbOH)
- Basa lemah :
- Amonium hidroksida (NH4OH)
- Aluminium hidroksida (Al(OH)3)
- Besi (III) hidroksida (Fe(OH)3)
- Amoniak (NH3)
- Besi (II) hidroksida (Fe(OH)2)
Teori Asam-Basa
1. Asam Basa Arrhenius
Teori ini pertama kalinya dikemukakan pada tahun 1884 oleh Svante August Arrhenius. Menurut Arrhenius, definisi dari asam dan basa, yaitu:
- Asam → zat yang dapat menghasilkan ion hidrogen (H+) jika dilarutkan ke dalam air.
- Basa → zat yang dapat menghasilkan ion hidroksida (OH−) jika dilarutkan ke dalam air.
Contoh:
↳ Reaksi ionisasi zat asam dalam air adalah sebagai berikut: 


↳ Reaksi ionisasi zat basa dalam air adalah sebagai berikut: 


2. Asam Basa Bronsted-Lowry
Pada tahun 1923, Johannes N. Brønsted dan Thomas M. Lowry secara terpisah mengajukan definisi asam dan basa yang lebih luas. Konsep yang diajukan tersebut didasarkan pada fakta bahwa reaksi asam–basa melibatkan transfer proton (ion H+) dari satu zat ke zat lainnya. Proses transfer proton ini selalu melibatkan asam sebagai pemberi/donor proton dan basa sebagai penerima/akseptor proton. Jadi, menurut definisi asam basa Brønsted–Lowry,
- Asam → zat yang memberikan H+ (donor proton)
- Basa → zat yang menerima H+ (akseptor elektron)

Contoh:
Jika ditinjau dengan teori Brønsted–Lowry, pada reaksi ionisasi HCl ketika dilarutkan dalam air, HCl berperan sebagai asam dan H2O sebagai basa.
HCl(aq) + H2O(l) → Cl−(aq) + H3O+(aq)
HCl berubah menjadi ion Cl− setelah memberikan proton (H+) kepada H2O. H2O menerima proton dengan menggunakan sepasang elektron bebas pada atom O untuk berikatan dengan H+ sehingga terbentuk ion hidronium (H3O+).

3. Asam Basa Lewis
Pada tahun 1923, G. N. Lewis mengemukakan teori asam basa yang lebih luas dibanding kedua teori sebelumnya dengan menekankan pada pasangan elektron yang berkaitan dengan struktur dan ikatan. Menurut definisi asam basa Lewis,
- Asam → zat yang menerima (akseptor) pasangan elektron.
- Basa → zat yang memberi (donor) pasangan elektron.
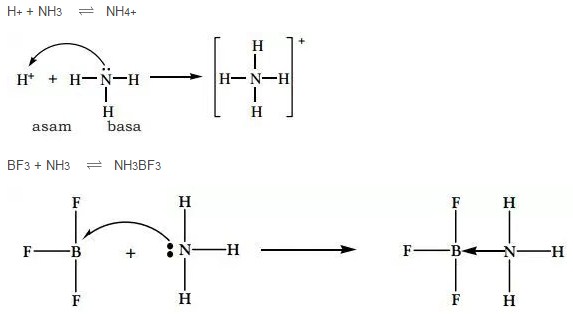
Contoh:

Contoh Teori Asam dan Basa Menurut Lewis pada Gambar diatas telah menunjukan bahwa Ion H+ (Proton) ialah Asam Lewis karena mampu menerima Pasangan Elektron, sedang NH3 merupakan Basa Lewis. Lalu pada reaksi antara BF3 dengan NH3 pada Gambar diatas yang merupakan Asam Lewis ialah BF3 karena bisa menerima sepasang Elektron dan teruntuk NH3 ialah Basa Lewis.
DAFTAR PUSTAKA:
Unknown. (2016, November 20). Apa itu Asam dan Basa. Dipetik Oktober 11, 2019, dari KitaCerdas.com: http://kitacerdas.com/asam-dan-basa/
Hady, E. (2011, Maret 22). Pengertian Asam, Basa dan Garam. Dipetik Oktober 11, 2019, dari Kompasian: https://www.kompasiana.com/1991/55009b8fa33311d3725118c8/pengertian-asam-basa-dan-garam
Nandini, A. W. (2015, Maret 29). Teori Asam dan Basa Arrhenius. Dipetik Oktober 11, 2019, dari Anggi Kimia Pasca UNP: https://anggiwilianandini.wordpress.com/kimia-kelas-xi/larutan-asam-basa/teori-asam-basa/teori-asam-dan-basa-arrhenius/
Nirwan Susianto, S. (t.thn.). Teori Asam Basa. Dipetik Oktober 11, 2019, dari Studio Belajar: https://www.studiobelajar.com/teori-asam-basa/
Reaven. (2017). Teori Asam dan Basa Menurut Arrhenius, Bronsted-Lowry, dan Lewis. Retrieved Oktober 11, 2019, from Myrightspot.com: https://www.myrightspot.com/2017/05/teori-asam-dan-basa-menurut-arrhenius-bronsted-lowry-lewis.html
Unknown. (2019, Juli 27). Teori Asam Basa Lewis di Dalam ilmu Kimia. Dipetik Oktober 11, 2019, dari RumusRumus.com: https://rumusrumus.com/teori-asam-basa-lewis/
DAFTAR PUSTAKA:
Unknown. (2016, November 20). Apa itu Asam dan Basa. Dipetik Oktober 11, 2019, dari KitaCerdas.com: http://kitacerdas.com/asam-dan-basa/
Hady, E. (2011, Maret 22). Pengertian Asam, Basa dan Garam. Dipetik Oktober 11, 2019, dari Kompasian: https://www.kompasiana.com/1991/55009b8fa33311d3725118c8/pengertian-asam-basa-dan-garam
Nandini, A. W. (2015, Maret 29). Teori Asam dan Basa Arrhenius. Dipetik Oktober 11, 2019, dari Anggi Kimia Pasca UNP: https://anggiwilianandini.wordpress.com/kimia-kelas-xi/larutan-asam-basa/teori-asam-basa/teori-asam-dan-basa-arrhenius/
Nirwan Susianto, S. (t.thn.). Teori Asam Basa. Dipetik Oktober 11, 2019, dari Studio Belajar: https://www.studiobelajar.com/teori-asam-basa/
Reaven. (2017). Teori Asam dan Basa Menurut Arrhenius, Bronsted-Lowry, dan Lewis. Retrieved Oktober 11, 2019, from Myrightspot.com: https://www.myrightspot.com/2017/05/teori-asam-dan-basa-menurut-arrhenius-bronsted-lowry-lewis.html
Unknown. (2019, Juli 27). Teori Asam Basa Lewis di Dalam ilmu Kimia. Dipetik Oktober 11, 2019, dari RumusRumus.com: https://rumusrumus.com/teori-asam-basa-lewis/



baguss
BalasHapusSangat lengkap👌
BalasHapus