Ikatan dan Unsur Kimia
IKATAN KIMIA
Selain gas mulia di alam, unsur-unsur tidak selalu berada sebagai unsur bebas (sebagai atom tunggal), tetapi kebanyakan bergabung dengan atom unsur lain. Tahun 1916 G.N. Lewis dan W. Kossel menjelaskan hubungan kestabilan gas mulia dengan konfigurasi elektron. Unsur gas mulia (golongan VIIIA) merupakan unsur yang paling stabil (artinya tidak mudah berubah atau tidak mudah bereaksi), karena mempunyai konfigurasi penuh, yaitu konfigurasi oktet (mempunyai 8 elektron terluar), kecuali Helium dengan konfigurasi duplet (2 elektron pada kulit terluar). Unsur-unsur selain gas mulia cenderung ingin stabil (memiliki konfigurasi oktet) dengan cara:
1. Melepaskan atau menangkap elektron
2.Penggunaan bersama pasangan elektron
Jenis-Jenis Ikatan Kimia
1. Ikatan Ion
Ikatan ion terbentuk akibat adanya melepas atau menerima elektron oleh atom-atom yang berikatan. Atom-atom yang melepas elektron menjadi ion positif (kation) sedang atom-atom yang menerima elektron menjadi ion negatif (anion). Ikatan ion biasanya disebut ikatan elektrovalen. Senyawa yang memiliki ikatan ion disebut senyawa ionik. Senyawa ionik biasanya terbentuk antara atom-atom unsur logam dan nonlogam. Atom unsur logam cenderung melepas elektron membentuk ion positif, dan atom unsur non-logam cenderung menangkap elektron membentuk ion negatif. Contoh: NaCl, MgO, CaF2, Li2O,AlF3, dan lain-lain.
Sifat-sifat senyawa yang berikatan ion :
- Titik didih dan titik lelehnya tinggi
- Keras, tetapi rapuh/mudah patah
- Penghantar panas yang baik
- Padatannya tidak menghantarkan listrik, tetapi lelehan dan larutannya dapat menghantarkan listrik
- Berwujud padat pada suhu kamar
- Larut dalam air, tetapi tidak larut dalam senyawa-senyawa organik, misalnya alkohol, benzena, dan petroleum eter
2. Ikatan Kovalen
Ikatan kovalen terjadi karena pemakaian bersama pasangan elektron oleh atom-atom yang berikatan. Pasangan elektron yang dipakai bersama disebut pasangan electron ikatan (PEI) dan pasangan elektron valensi yang tidak terlibat dalam pembentukan ikatan kovalen disebut pasangan elektron bebas (PEB).
Ikatan kovalen umumnya terjadi antara atom-atom unsur nonlogam, bisa sejenis (contoh: H2, N2, O2,Cl2, F2, Br2, I2) dan berbeda jenis (contoh: H2O, CO2, dan lain-lain). Senyawa yang hanya mengandung ikatan kovalen disebut senyawa kovalen. Berdasarkan lambang titik Lewis dapat dibuat struktur lewis atau rumus lewis. Struktur Lewis adalah penggambaran ikatan kovalen yang menggunakan lambang titik Lewis di mana PEI dinyatakan dengan satu garis atau sepasang titik yang diletakkan di antara kedua atom dan PEB dinyatakan dengan titik-titik pada masing-masing atom.
Berdasarkan jumlah PEI (Pasangan Elektron Ikatan), ikatan kovalen dibagi atas 3 :
a. Ikatan kovalen tunggal yaitu ikatan kovalen yang memiliki 1 pasang PEI. Contoh : H2
b. Ikatan kovalen rangkap dua yaitu ikatan kovalen yang memiliki 2 pasang PEI. Contoh : O2
c. Ikatan kovalen rangkap tiga yaitu ikatan kovalen yang memiliki 3 pasang PEI. Contoh : N2
Berdasarkan kepolaran ikatan, ikatan kovalen dibagi 2:
- Ikatan kovalen polar
Ikatan kovalen polar adalah ikatan kovalen yang PEI-nya cenderung tertarik ke salah satu atom yang berikatan. Kepolaran suatu ikatan kovalen ditentukan oleh keelektronegatifan suatu unsur. Senyawa kovalen polar biasanya terjadi antara atom-atom unsur yang beda keelektronegatifannya besar, mempunyai bentuk molekul asimetris, mempunyai momen dipol (μ = hasil kali jumlah muatan dengan jaraknya) ≠0.
Contoh :
H2O : Keelektronegatifan 2,1 : 3,5, beda keelektronegatifan = 3,5 – 2,1 = 1,4
NH3 : Keelektronegatifan 2,1 : 3,0, beda keelektronegatifan = 3,0 – 2,1 = 0,9
- Ikatan Kovalen Nonpolar
Ikatan kovalen nonpolar yaitu ikatan kovalen yang PEI-nya tertarik sama kuat ke arah atom-atom yang berikatan. Senyawa kovalen nonpolar terbentuk antara atom-atom unsur yang mempunyai beda keelektronegatifan nol atau mempunyai momen dipol = 0 atau mempunyai bentuk molekul simetri. Contoh :
CH4 : Beda keelektronegatifan 2,1 : 2,5 maka beda keelektronegatifan = 2,5 – 2,1 = 0,4 dan bentuk molekul simetri.
- Ikatan kovalen koordinasi
Ikatan kovalen koordinasi adalah ikatan kovalen yang PEI-nya berasal dari salah satu atom yang berikatan.
Sifat-sifat senyawa yang berikatan kovalen :
- Pada suhu kamar berwujud gas, cair (Br2), dan ada yang padat (I2)
- Padatannya lunak dan tidak rapuh.
- Mempunyai titik didih dan titik leleh rendah.
- Larut dalam pelarut organik tapi tidak larut dalam air.
- Umumnya tidak menghantarkan listrik.
3. Ikatan Logam
Ikatan logam adalah ikatan kimia yang terbentuk akibat penggunaan bersama elektron-elektron valensi antar atom-atom logam. Contoh: logam besi, seng, dan perak. Ikatan logam bukanlah ikatan ion atau ikatan kovalen. Salah satu teori yang dikemukakan untuk menjelaskan ikatan logam adalah teori lautan elektron. Contoh terjadinya ikatan logam. Tempat kedudukan elektron valensi dari suatu atom besi (Fe) dapat saling tumpang tindih dengan tempat kedudukan elektron valensi dari atom-atom Fe yang lain. Tumpang tindih antar elektron valensi ini memungkinkan elektron valensi dari setiap atom Fe bergerak bebas dalam ruang di antara ion-ion Fe+ membentuk lautan elektron. Karena muatannya berlawanan (Fe2+ dan 2e–), maka terjadi gaya tarik-menarik antara ion-ion Fe+ dan elektron-elektron bebas ini. Akibatnya terbentuk ikatan yang disebut ikatan logam.
FAKTOR GEOMETRI
Jari-jari atom dan kekuatan menarik elektron atom atau ion menentukan ikatan, struktur, dan reaksi zat elementer senyawa.
1. Jari-Jari Atomik dan Ionik
→ Jari-Jari Atom
Kerapatan elektron dalam atom secara perlahan akan menuju, tetapi tidak pernah mencapai nol ketika jarak dari inti meningkat. Oleh karena itu, secara ketat dapat dinyatakan bahwa jari-jari atom atau ion tidak dapat ditentukan. Namun, secara eksperimen mungkin untuk menentukan jarak antar inti atom. Jari-jari atomik yang ditentukan secara eksperimen merupakan salah satu parameter atomik yang sangat penting untuk mendeskripsikan kimia struktural senyawa. Cukup beralasan untuk mendefinisikan jari-jari logam sebagai separuh jarak atom logam. Separuh jarak antar atom didefinisikan juga sebagai jari-jari kovalen zat elementer (Tabel 2-1).
→Jari-Jari Ionik
Karena kation dan anion unsur yang berbeda dalam senyawa ion diikat dengan interaksi elektrostatik, jarak ikatan adalah jumlah jari-jari ionik yang diberikan untuk kation dan anion.
Jari-jari ionik standar satu spesies ditetapkan terlebih dahulu dan kemudian dikurangkan dari jarak antar ion untuk menentukan jari-jari ion partnernya. Sebagai standar, jari-jari ion O2- dalam sejumlah oksida ditetapkan sebesar 140 pm (1 pm = 10-12 m) (R. D. Shannon).
2. Entalpi Kisi
Ketika ion-ion dalam keadaan gas bereaksi satu dengan yang lainnya membentuk senyawa kemudian melepaskan entalpi atau mengubah nilai entalpi, itulah yang disebut entalpi kisi. Sebagai contoh adalah pembentukan NaCl yang biasanya melepaskan kalor ke lingkungan:
3. Tetapan Madelung
Energi potensial Coulomb total antar ion dalam senyawa ionik yang terdiri atas ion A dan B adalah penjumlahan energi potensial Coulomb interaksi ion individual, Vab. Karena lokasi ion-ion dalam kisi kristal ditentukan oleh tipe struktur, potensial Coulomb total antar ion dihitung dengan menentukan jarak antar ion d. A adalah tetapan Madelung yang khas untuk tiap struktur kristal (Tabel 2-3).
NA adalah tetapan Avogadro dan zA dan zB adalah muatan listrik kation dan anion. Interaksi elektrostatik antara ion-ion yang bersentuhan merupakan yang terkuat, dan tetapan Madelung biasanya menjadi lebih besar bila bilangan koordinasinya meningkat. Sebab muatan listrik mempunyai tanda yang berlawanan, potensialnya menjadi negatif, menunjukkan penstabilan yang menyertai pembentukan kisi kristal dari ion-ion fasa gas yang terdispersi baik. Walaupun potensial listrik terendah biasanya menghasilkan struktur paling stabil, namun ini tidak selalu benar sebab ada interaksi lain yang harus dipertimbangkan.
Faktor terbesar selanjutnya yang berkontribusi pada entalpi kisi adalah gaya van der Waals, dan gaya dispersi atau interaksi London. Interaksi ini bersifat tarikan antara dipol listrik, yang berbanding terbalik dengan pangkat 6 jarak antar ion. Gaya van der Waals nilainya sangat kecil.
4. Struktur Kristal Logam
Di bagian kiri terjauh merupakan bentuk kubik (bcc= Body Centered Cubic) struktur berpusat badan. Dalam kristal itu, atom logam menempati delapan sudut kubus bersama dengan satu atom di pusat. Jumlah koordinasi setiap atom dalam struktur kubus berpusat badan adalah 8. Dalam bentuk kubik (fcc=Face Cetered Cubic) struktur kubus berpusat muka, ada delapan atom pada setiap sudut kubus dan enam atom di tengah wajah masing-masing. Jumlah koordinasi setiap atom dalam struktur kubus berpusat muka adalah 12. Heksagonal tumpukan padat (hcp=Hexagonal Close Packed) Struktur ini juga memiliki jumlah koordinasi 12, tapi kristal jenis ini berbentuk heksagonal dan bukan kubuk.
5. Kristal Ionik
Kristal ionik terbentuk karena adanya gaya tarik antara ion bermuatan positif dan negatif. Umumnya, kristal ionik memiliki titik leleh tinggi dan hantaran listrik yang rendah. Contoh dari kristal ionik adalah NaCl. Kristal ionik tidak memiliki arah khusus seperti kristal kovalen sehingga pada kristal NaCl misalnya, ion natrium akan berinteraksi dengan semua ion klorida dengan intensitas interaksi yang beragam dan ion klorida akan berinteraksi dengan seluruh ion natriumnya.
6. Aturan Jari-Jari
Biasanya, energi potensial Coulomb total Ec senyawa ionik univalen MX diungkapkan dengan persamaan
NA adalah konstanta Avogadro, A konstanta Madelung dan R jarak antar ion. Menurut rumus ini, struktur dengan rasion A/R akan lebih stabil. Konstanta Madelung senyawa MX meningkat dengan meningkatnya bilangan koordinasi. Di pihak lain, akan menguntungkan menurunkan bilangan koordinasi untuk menurunkan nilai R dalam hal ukuran M kecil, agar kontak antara M dan X dapat terjadi lebih baik. Dalam kristal ionik, rasio rM dan rX dengan anion saling kontak satu sama lain dan juga berkontak dengan kation bergantung pada bilangan koordinasi.
Dalam bagian struktur yang terdiri hanya anion, anion membentuk koordinasi polihedra di sekeliling kation. Jari-jari anion rX adalah separuh sisi polihedral dan jarak kation di pusat polihedral ke sudut polihedral adalah jumlah jari-jari kation dan anion rX + rM. Polihedra dalam CsCl adalah kubus, struktur NaCl adalah oktahedral, dan ZnS adalah tetrahedral. Jarak dari pusat ke sudut polihedral adalah berturut-turut √3rX, √2 rX dan ½√6rX. Sehingga, rasio jari-jari kation dan anion adalah are (√3rX-rX)/ rX = √3-1 = 732 untuk CsCl, (√2rX-rX)/ rX = √2-1 = 0.414 untuk NaCl, dan (½√6rX-rX)/ rX = ½√6-1 = 0.225 untuk ZnS ( Gambar di bawah).
Telah dijelaskan bahwa bilangan koordinasi menurun bila rasio jari-jari lebih kecil dari nilai yang diberikan sebab kation dan anion tidak bersentuhan satu sama lain, yang menyebabkan ketidakstabilan. Di lain pihak, bilangan koordinasi meningkat untuk kation yang lebih besar, yang akan meningkatkan rasio jari-jari. Namun demikian, hubungan antara bilangan koordinasi dan rasio jari-jari tidak sederhana. Misalnya, semua halida logam alkali mengadopsi struktur NaCl pada suhu normal kecuali cesium khlorida CsCl, cesium bromida CsBr dan cesium iodida CsI. Tidak dimungkinkan untuk menetapkan struktur ion dari rasio jari-jari bahkan untuk senyawa yang paling sederhana seperti alkali halida sekalipun. Namun, kecenderungan kualitatif bahwa ion yang lebih kecil cenderung berkoordinasi dengan lebih sedikit ion lawan biasanya benar.
7. Variasi Ungkapan Struktur Padatan
Banyak padatan anorganik memiliki struktur 3-dimensi yang rumit. Ilustrasi yang berbeda dari senyawa yang sama akan membantu kita memahami struktur tersebut. Dalam hal senyawa anorganik yang rumit, menggambarkan ikatan antar atom, seperti yang digunakan dalam senyawa organik biasanya menyebabkan kebingungan. Anion dalam kebanyakan oksida, sulfida atau halida logam membentuk tetrahedral atau oktahedral di sekeliling kation logam. Walaupun tidak terdapat ikatan antar anion, strukturnya akan disederhanakan bila struktur diilustrasikan dengan polihedra anion yang menggunakan bersama sudut, sisi atau muka. Dalam ilustrasi semacam ini,atom logam biasanya diabaikan.
Seperti telah disebutkan struktur ionik dapat dianggap sebagai susunan terjejal anion. Gambar 2.12 dan 2-13 mengilustrasikan ketiga representasi ini untuk fosfor pentoksida molekular P2O5 (= P4O10) dan molibdenum pentakhlorida MoCl5 (= Mo2Cl10). Representasi polihedra jauh lebih mudah dipahami untuk struktur molekul besar atau padatan yang dibentuk oleh tak hingga banyaknya atom. Namun, representasi garis ikatan juga cocok untuk senyawa molekular.
FAKTOR ELEKTRONIK
Ikatan dan struktur senyawa ditentukan oleh sifat elektronik seperti kekuatan atom-atom penyusun dalam menarik dan menolak elektron. Orbital molekul yang diisi elektron elektron valensi, susunan geometrisnya dipengaruhi oleh interaksi elektronik antar elektron non ikatan.
1. Muatan Inti Efektif
Muatan inti efektif (Zeff) adalah muatan total dari inti atom yang dirasakan oleh elektron terluar. Muatan inti efektif mempengaruhi jari-jari atom, energi ionisasi dan afinitas elektron.
Konstanta perisai merupakan konstanta yang dihasilkan efek perisai (efek yang “melindungi” sebagian terhadap gaya tarik inti akibat elektron-elektron pada kulit redah), besarnya konstanta perisai (σ) lebih besar dari nol tetapi lebih kecil dari Z.
2. Energi Ionisasi
Energi ionisasi, adalah energi minimum (kJ/mol) yang diperlukan untuk melepaskan satu elektron dari atom gas pada keadaan dasar. Energi ionisasi ditekankan pada pembentukan ion bermuatan positif. Semakin besar ukuran/nomor atom, maka semakin mudah atom melepaskan elektron, sehingga semakin mudah membentuk ion bermuatan positif. Semakin besar nilai energi ionisasi, maka semakin sulit elektron dilepaskan dari atom.

3. Afinitas Elektron
Afinitas elektron, negatif dari perubahan energi yang terjadi ketika suatu elektron ditangkap oleh suatu atom dalam keadaan gas untuk membentuk ion. Unsur dengan afinitas elektron bertanda negatif memiliki kecenderungan lebih besar dalam menyerap elektron daripada unsur dengan afinitas elektron bertanda positif. Semakin negatif nilai afinitas elektron, maka semakin besar kemampuan unsur dalam menyerap elektron, sehingga semakin besar kemampuan unsur untuk membentuk ion bermuatan negatif.
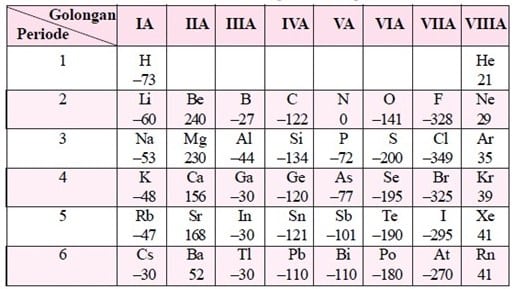
Kecenderungan sifatnya semakin ke kanan dalam satu periode, semakin besar energi ionisasinya, semakin ke bawah dalam satu golongan energi ionisasinya semakin kecil.
4. Ke-Elektronegatifan


DAFTAR PUSTAKA
1. Muatan Inti Efektif
Muatan inti efektif (Zeff) adalah muatan total dari inti atom yang dirasakan oleh elektron terluar. Muatan inti efektif mempengaruhi jari-jari atom, energi ionisasi dan afinitas elektron.
Zeff = Z - S
Keterangan :
Z = Jumlah proton dalam inti atom atau nomor atom.
S = Konstanta perisai
2. Energi Ionisasi
Energi ionisasi, adalah energi minimum (kJ/mol) yang diperlukan untuk melepaskan satu elektron dari atom gas pada keadaan dasar. Energi ionisasi ditekankan pada pembentukan ion bermuatan positif. Semakin besar ukuran/nomor atom, maka semakin mudah atom melepaskan elektron, sehingga semakin mudah membentuk ion bermuatan positif. Semakin besar nilai energi ionisasi, maka semakin sulit elektron dilepaskan dari atom.

Dinyatakan bahwa :
- Dalam satu golongan, dari atas ke bawah, energi ionisasi akan semakin kecil.
- Dalam satu periode, dari kiri ke kanan, energi ionisasi akan semakin besar.
Energi ionisasi dinyatakan dalam satuan internasional, yaitu elektron volt (eV) dengan nilai 1 eV = 1,60 x 10-19 J = 96,485 kJ.mol-1. Dengan batasan tersebut dinyatakan bahwa energi ionisasi bergantung pada seberapa kuat elektron terikat pada atom atau seberapa kuat muatan inti efektifnya.
3. Afinitas Elektron
Afinitas elektron, negatif dari perubahan energi yang terjadi ketika suatu elektron ditangkap oleh suatu atom dalam keadaan gas untuk membentuk ion. Unsur dengan afinitas elektron bertanda negatif memiliki kecenderungan lebih besar dalam menyerap elektron daripada unsur dengan afinitas elektron bertanda positif. Semakin negatif nilai afinitas elektron, maka semakin besar kemampuan unsur dalam menyerap elektron, sehingga semakin besar kemampuan unsur untuk membentuk ion bermuatan negatif.

Kecenderungan sifatnya semakin ke kanan dalam satu periode, semakin besar energi ionisasinya, semakin ke bawah dalam satu golongan energi ionisasinya semakin kecil.
4. Ke-Elektronegatifan
- L. Pauling
Tokoh kimia yang menemukan rancangan skala keelektronegatifan adalah Linus Pauling. Karena jasanya maka muncul yang dinamakan Skala Keelektronegatifan Pauling. Pauling menggunakan konsep kekuatan ikatan yang disebabkan dari adanya ikatan kovalen antar atom yang diperkuat dengan gaya tarik-menarik antar muatan yang berlawanan dari ikatan dipol.

Berdasarkan tabel skala keelektronegatifan kita dapat menentukan jenis ikatan dan sifat suatu senyawa. Perbedaan keelektronegatifan dapat digunakan untuk menentukan polaritas suatu ikatan.Perbedaan keelektronegatifan yang kecil menghasilkan ikatan yang bersifat non polar. Sedangkan perbedaan keelektronegatifan yang besar menjadikan senyawa bersifat ion sempurna.
- A. L. Allerd dan E. G. Rochow
Allred dan Rochow beranggapan[11] bahwa elektronegativitas haruslah berhubungan dengan muatan sebuah elektron pada "permukaan" sebuah atom: semakin tinggi muatan per satuan lebar permukaan atom, semakin agung kecenderungan atom tersebut untuk menarik elektron-elektron. Muatan inti efektif, Z* yang terdapat pada elektron valensi dapat diperkirakan dengan memakai kaidah Slater. Sedangkan lebar permukaan atom pada sebuah molekul dapat dihitung dengan asumsi lebar ini proposional dengan kuadrat jari-jari kovalen (rcov). rcov memiliki satuan ångström,
- R. Mulliken
Mulliken mengajukan bahwa purata aritmetik dari energi ionisasi pertama dan afinitas elektron haruslah adalah sebuah hitungan dari kecenderungan sebuah atom menarik elektron-elektron. Sebab arti ini tidak bergantung pada skala relatif sembarang, ia juga dikata sebagai elektronegativitas relatif, dengan satuan kilojoule per mol atau elektronvolt.
4. Orbital Molekul
Sifat simetri dan energi relatif orbital atom menentukan bagaimana mereka berinteraksi untuk membentuk orbital molekul. Orbital molekul ini kemudian diisi dengan elektron tersedia sesuai dengan aturan yang sama yang digunakan untuk orbital atom, dan energi total elektron dalam orbital molekul dibandingkan dengan total awal energi elektron dalam orbital atom.
Koefisien bisa sama atau tidak sama, positif atau negatif, tergantung pada orbital individu dan energi mereka. Sebagai jarak antara dua atom menurun, orbital mereka tumpang tindih, probabilitas signifikan Wilh untuk elektron dari kedua atom di wilayah tumpang tindih. Akibatnya, orbital molekul bentuk. Elektron dalam ikatan orbital molekul menempati ruang antara inti, dan gaya elektrostatik antara elektron dan dua inti positif terus atom bersama-sama.
Tiga kondisi penting untuk tumpang tindih menyebabkan ikatan :
a. Simetri orbital harus sedemikian rupa sehingga daerah dengan tanda yang sama tumpang tindih Ψ.
b. Energi orbital atom harus sama. Ketika energi berbeda dengan jumlah yang besar, perubahan energi pada pembentukan orbital molekul kecil dan pengurangan net energi elektron terlalu kecil untuk ikatan yang signifikan.
c. Jarak antara atom harus cukup pendek untuk memberikan tumpang tindih baik dari orbital, tapi tidak begitu singkat bahwa pasukan menjijikkan elektron lain atau inti mengganggu.

DAFTAR PUSTAKA
Budiatma, H. (2019, February 14). Struktur Kristal Logam. Retrieved September 16, 2019, from Usaha321: https://usaha321.net/struktur-kristal-logam.html
elDjanbie, M. F. (2012, February 22). Kamu tahukan aturan jari-jari. Retrieved September 16, 2019, from BANK KIMIA: http://bankimia.blogspot.com/2012/02/kamu-tahukan-aturan-jari-jari.html
Mulyono. (2011, October 15). Variasi ungkapan struktur padatan. Retrieved September 16, 2019, from Mulyono Blog's: http://sersan-mulyono.blogspot.com/2011/10/variasi-ungkapan-struktur-padatan.html
Suharni, R. (2016, February 17). Ikatan Kimia. Retrieved September 16, 2019, from The World of Chemistry: https://ranisuharni.wordpress.com/kimia-kelas-x/ikatan-kimia/
K., L. R. (2018, Februari 18). Muatan Inti Efektif, Jari-Jari Atom, Energi Ionisasi, Afinitas Elektron Dan Keelektronegatifan. Dipetik Oktober 8, 2019, dari Brankas: https://ratukemalalaura.blogspot.com/2018/02/muatan-inti-efektif-jari-jari-atom.html
Khaderyamulva. (2017, Januari 25). Muatan inti efektif. Dipetik Oktober 8, 2019, dari Khaderya's blog: http://khaderyamulva.blogspot.com/2017/01/muatan-inti-efektif.html
Unknown. (2018, Agustus 7). Apa itu Keelektronegatifan? Dipetik Oktober 8, 2019, dari GreatEdu: https://greatedu.co.id/greatpedia/apa-itu-keelektronegatifan
Unknown. (n.d.). Elektronegativitas. Retrieved Oktober 8, 2019, from ELEKTRONEGATIVITAS: http://m.portal-fisika.gilland-ganesha.com/ind/2875 2762/Elektronegativitas_22810_unusumbar_portal-fisika-unusumbar.html
K., L. R. (2018, Februari 18). Muatan Inti Efektif, Jari-Jari Atom, Energi Ionisasi, Afinitas Elektron Dan Keelektronegatifan. Dipetik Oktober 8, 2019, dari Brankas: https://ratukemalalaura.blogspot.com/2018/02/muatan-inti-efektif-jari-jari-atom.html
Khaderyamulva. (2017, Januari 25). Muatan inti efektif. Dipetik Oktober 8, 2019, dari Khaderya's blog: http://khaderyamulva.blogspot.com/2017/01/muatan-inti-efektif.html
Unknown. (2018, Agustus 7). Apa itu Keelektronegatifan? Dipetik Oktober 8, 2019, dari GreatEdu: https://greatedu.co.id/greatpedia/apa-itu-keelektronegatifan
Unknown. (n.d.). Elektronegativitas. Retrieved Oktober 8, 2019, from ELEKTRONEGATIVITAS: http://m.portal-fisika.gilland-ganesha.com/ind/2875 2762/Elektronegativitas_22810_unusumbar_portal-fisika-unusumbar.html



















👍👍👍👍
BalasHapusMantul
BalasHapusBaguss
BalasHapusbaguss kakk
BalasHapusNtaps
BalasHapusBagus bgttt
BalasHapusMantep
BalasHapusMantep
BalasHapusBagus👍
BalasHapusBaguss👌
BalasHapusGood
BalasHapusSangat lengkap👌
BalasHapus